Chlorek glinu
| ||||||||||||||||||||||||||||||||||||||||||||
 Próbki białego i żółtego AlCl 3·6H 2O ([Al(H 2O) 6]Cl 3) | ||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | AlCl3 | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 133,34 g/mol | |||||||||||||||||||||||||||||||||||||||||||
| Wygląd | białe lub żółte ciało stałe | |||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 7446-70-0 | |||||||||||||||||||||||||||||||||||||||||||
| PubChem | 24012 | |||||||||||||||||||||||||||||||||||||||||||
| DrugBank | 11081 | |||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||||
| Inne aniony | trichlorek boru | |||||||||||||||||||||||||||||||||||||||||||
| Inne kationy | fluorek glinu | |||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | chlorek żelaza(III), fluorek boru | |||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||||
| Klasyfikacja medyczna | ||||||||||||||||||||||||||||||||||||||||||||
| ATC | D10 AX01 | |||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
Chlorek glinu, AlCl3 – nieorganiczny związek chemiczny, sól kwasu solnego i glinu. Jest białym ciałem stałym[6] (produkty handlowe mogą mieć zabarwienie żółte[2]). Związek bezwodny dymi na powietrzu z powodu hydrolizy spowodowanej parą wodną. Jest kwasem Lewisa i stosowany jest głównie jako katalizator w reakcji Friedla-Craftsa[4].
Struktura
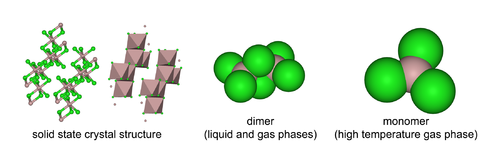
W stanie stałym chlorek glinu ma budowę krystaliczną o strukturze warstwowej, w której glin ma liczbę koordynacyjną 6[4]. W stanie ciekłym i gazowym (poniżej 400 °C) jest dimerem, Al2Cl6, zaś w wysokiej temperaturze przyjmuje formę monomeru, AlCl3 (forma wyłączna powyżej 800 °C)[3].
Heksahydrat ma charakter soli kompleksowej [Al(H
2O)
6]Cl
3[7].
Otrzymywanie
Bezwodny chlorek glinu otrzymuje się m.in. w reakcji glinu z chlorem lub chlorowodorem[8]:
- 2Al + 3Cl
2 → 2AlCl
3 (podstawowa metoda przemysłowa)[3] - 2Al + 6HCl → 2AlCl
3 + 3H
2
Inną metodą przemysłową jest chlorowanie tlenku glinu mieszaniną chloru i tlenku węgla[3].
Heksahydrat można uzyskać rozpuszczając tlenek glinu w kwasie solnym, a w formie krystalicznej – przepuszczając HCl przez nasycony roztwór związku[3].
Właściwości fizyczne
Chlorek glinu przy ogrzewaniu pod normalnym ciśnieniem sublimuje przy 180 °C. Pod zwiększonym ciśnieniem topi się w temperaturze ok. 192 °C, czemu towarzyszy gwałtowny spadek przewodnictwa elektrycznego i wzrost objętości o 85%. Wynika to ze zmiany struktury podczas przemiany fazowej[4][7].
Właściwości chemiczne
Chlorek glinu reaguje bardzo gwałtownie z wodą tworząc heksahydrat, AlCl
3·6H
2O, hydrolizujący do tlenochlorku glinu, AlClO, i kwasu solnego, w wyniku czego roztwór ma charakter silnie kwasowy[3]. Ogrzewanie heksahydratu prowadzi do wydzielenia chlorowodoru, pary wodnej i tlenku glinu (Al
2O
3)[8].
Zastosowanie
Chlorek glinu stosuje się jako katalizator w syntezie organicznej (np. w reakcji Friedla-Craftsa)[8]:
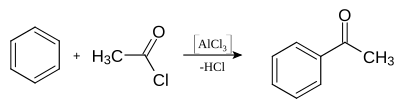
Reakcja Friedla-Craftsa z udziałem chlorku glinu jako katalizatora
Jest on również stosowany do wyrobu papieru pergaminowego, a także w garbarstwie i medycynie[8].
Przypisy
- ↑ a b Chlorek glinowy w katalogu Merck Chemicals. [dostęp 2011-03-07]. (pol.).
- ↑ a b Chlorek glinu (nr 563919) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski.
- ↑ a b c d e f Otto Helmboldt, L. Keith Hudson, Chanakya Misra, Karl Wefers, Wolfgang Heck, Hans Stark, Max Danner, Norbert Rösch. Aluminum Compounds, Inorganic. „Ullmann's Encyclopedia of Industrial Chemistry”, 2007. DOI: 527.pub2 10.1002/14356007.a01 527.pub2.
- ↑ a b c d N. N. Greenwood, A. Earnshaw: Chemistry of the elements. Oxford; New York: Pergamon Press, 1984, s. 262-266. ISBN 0-08-022057-6.
- ↑ a b Chlorek glinu, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-04-10] (ang.).
- ↑ Dale L. Perry: Handbook of inorganic compound. Boca Raton: Taylor Francis, 2011, s. 5. ISBN 978-1-4398-1461-1.
- ↑ a b Adam Bielański: Podstawy chemii nieorganicznej. Wyd. 5. Warszawa: PWN, 2002, s. 789. ISBN 83-01-13654-5.
- ↑ a b c d Podręczny słownik chemiczny, RomualdR. Hassa (red.), JanuszJ. Mrzigod (red.), JanuszJ. Nowakowski (red.), Katowice: Videograf II, 2004, s. 72, ISBN 83-7183-240-0 .
- p
- d
- e
| 1. Litowców | |
|---|---|
| 2. Berylowców |
|
| 3. Skandowców |
|
| 4. Tytanowców |
|
| 5. Wanadowców |
|
| 6. Chromowców |
|
| 7. Manganowców |
|
| 8. Żelazowców |
|
| 9. Kobaltowców |
|
| 10. Niklowców |
|
| 11. Miedziowców |
|
| 12. Cynkowców |
|
| 13. Borowców |
|
| 14. Węglowców |
|
| 15. Azotowców |
|
| 16. Tlenowców |
|
| 17. Fluorowców |
|
- p
- d
- e
- p
- d
- e
| D10A – Leki przeciwtrądzikowe do stosowania zewnętrznego |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| D10B – Leki do stosowania wewnętrznego |
|
 Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
- Britannica: science/aluminum-trichloride
- SNL: aluminiumklorid
- Catalana: 0220796












